Les anticorps monoclonaux sont un pool d'anticorps spécifiques du même épitope car ils sont initialement produits par une seule cellule lymphocytaire B. Comme pour les anticorps polyclonaux, un animal hôte doit d'abord être immunisé pour recevoir la cellule productrice d'anticorps (voir figure 1, étapes 1 et 2). Cette cellule est ensuite fusionnée avec une cellule tumorale du même hôte (voir la figure 1 étape 4).
En 1975, G. Köhler et C. Milstein ont publié dans Nature l'introduction de la technique de l'hybridome pour produire des anticorps monoclonaux.1 Cette technique est devenue un pilier de la science biologique moderne, du diagnostic des maladies et de la thérapie actuelle de diverses maladies. Les auteurs ont fusionné un myélome de souris avec une cellule de rate de souris (tous deux d'origine BALB/c) pour obtenir un certain nombre de lignées cellulaires sécrétant des anticorps contre des globules rouges de mouton (voir figure 1 étape 4 et 5). Le résultat de cette fusion était une lignée cellulaire hybride, appelée hybridome, qui exprimait de manière stable des anticorps monoclonaux. Les cellules d'hybridome pouvaient ensuite être injectées à des souris BLAB/c pour produire un sérum spécifique de l'antigène ou hybridées à des cellules productrices d'anticorps de différentes origines pour induire la production in vitro d'anticorps. Georges Köhler, César Milstein et Niels Kaj Jerne se sont partagés le prix Nobel de physiologie ou de médecine en 1984 pour cette découverte.
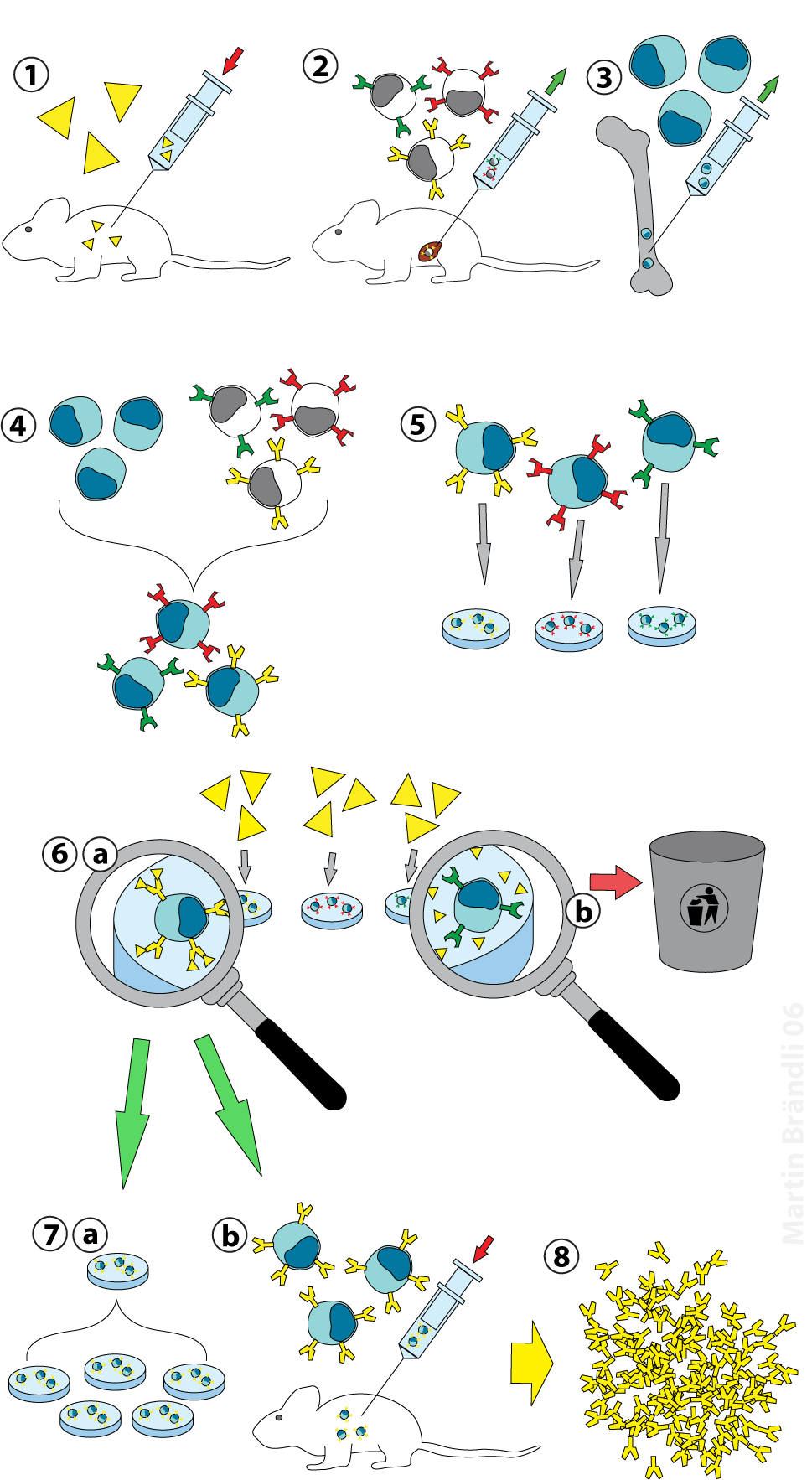
Fig 1 : Principe de la technique de l'hybridome Martin Brändli (Own work) [CC-BY-SA-2.5 (http://creativecommons.org/licenses/by-sa/2.5)], via Wikimedia Commons
Les cellules hybridomes synthétisent l'anticorps monoclonal spécifique produit à l'origine par la cellule lymphocytaire B. La cellule lymphocytaire B d'origine produira l'anticorps monoclonal en fonction de l'antigène qui a été injecté à l'hôte avant la récolte des cellules lymphocytaires B. Si, par exemple, l'hôte est exposé à un virus en réplication, il développera des lymphocytes B qui produiront des anticorps viraux spécifiques. La fusion avec une cellule tumorale pour fabriquer l'hybridome entraîne la production d'anticorps monoclonaux contre le virus spécifique.
Les cellules d'hybridome sont ensuite sélectionnées par affinité épitopique et après un autre tour dans une culture sélective en milieu hypoxanthine-aminoptérine-thymidine (milieu HAT). L'aminoptérine bloque la synthèse de novo de l'ADN, nécessaire à la division cellulaire, tandis que l'hypoxanthine et la thymidine fournissent aux cellules la matière première nécessaire pour contourner le blocage si la cellule héberge les enzymes fonctionnelles essentielles. Les cellules myélomateuses non fusionnées ne produisent pas les bonnes enzymes, tandis que les cellules spléniques non fusionnées ne peuvent pas se développer indéfiniment. Ainsi, seules les cellules d'hybridome se développeront indéfiniment dans le milieu.2
Comme décrit ci-dessus, il existe deux méthodes pour cultiver des cellules d'hybridome (ici décrites pour la souris hôte commune) : 1) les injecter dans la cavité péritonéale d'une souris (voir Figure 1 étape 7b) ou 2) utiliser des techniques de culture cellulaire in vitro (voir Figure 1 étape 7a). La technique de culture cellulaire nécessite une certaine expertise, des milieux spéciaux, et peut être coûteuse et longue. Bien que la méthode de culture cellulaire soit largement préférée, un certain nombre d'anticorps monoclonaux seront encore produits in vivo chez la souris. Lorsqu'elles sont injectées dans une souris, les cellules d'hybridome se multiplient et produisent du liquide (ascite) dans son abdomen ; ce liquide contient une forte concentration d'anticorps (souvent une concentration 10 fois supérieure à celle obtenue dans les surnageants de culture cellulaire).2 Le comité institutionnel de soins et d'utilisation des animaux (IACUC) a créé une directive, dans quelles conditions la production in vivo d'anticorps monoclonaux est acceptable.3
Les anticorps monoclonaux sont désormais largement utilisés pour la recherche, le diagnostic et les thérapies. Un inconvénient des anticorps de souris couramment utilisés pour les applications thérapeutiques est la réponse immunitaire humaine en raison des différences structurelles mineures entre les anticorps humains et murins. En 1988, Greg Winter et son équipe ont été les premiers à mettre au point des techniques permettant d'humaniser les anticorps monoclonaux, minimisant ainsi les réactions que de nombreux anticorps monoclonaux provoquaient chez les patients.4 Dans l'une des approches, l'ADN de souris codant pour la portion de liaison d'un anticorps monoclonal a été recombiné avec l'ADN produisant des anticorps humains dans des cellules vivantes. Cela a donné des anticorps monoclonaux partiellement murins, partiellement humains lorsqu'ils ont été exprimés dans une culture cellulaire. Ces produits sont appelés anticorps chimériques.5 A présent, les anticorps chimériques peuvent être produits dans diverses espèces hôtes, pas seulement la souris et l'homme.
De nombreuses cibles protéiques liées à la transduction du signal et aux maladies sont hautement conservées entre les souris, les humains et les rats. Elles peuvent donc être reconnues comme des auto-antigènes si l'hôte est un rat ou une souris et sont par conséquent moins immunogènes. Jusqu'à présent, un certain nombre d'hybridomes provenant de différents animaux hôtes ont été introduits pour surmonter les limites de la reconnaissance des antigènes chez la souris. D'autre part, les antigènes végétaux sont parfois moins immunogènes chez les herbivores et les omnivores ou carnivores sont donc mieux armés pour produire de tels antigènes.
Info: antibodies-online.com propose plus de 100.000 anticorps monoclonaux.
Anticorps monoclonaux en vedette
- (122)
- (8)
- (4)
- (4)
- (2)
- (8)
- (15)
- (1)
- (67)
- (34)
- (126)
- (12)
- (7)
- (1)
- (10)
- (1)
- (7)
- (2)
- (3)
- (4)
- (1)
- (6)
- (2)
Références :
1 Köhler, G. & Milstein, C. (1975): Continuous cultures of fused cells secreting antibody of predefined specificity. In: Nature. Bd. 256, S. 495–497. PMID 1172191. doi:10.1038/256495a0, Nachdruck in: J. Immunol. Bd. 174, S. 2453–2455. PMID 15728446
2 Monoclonal Antibody Production; National Research Council (US) Committee on Methods of Producing Monoclonal Antibodies. Washington (DC): National Academies Press (US); 1999. ISBN-10: 0-309-07511-4 ISBN-13: 978-0-309-07511-4 ISBN-10: 0-309-51904-7, Available from: http://www.ncbi.nlm.nih.gov/books/NBK100200/
3 http://iacuc.utk.edu/policies-and-procedures/guidelines-for-in-vivo-monoclonal-antibody-production/
4 Riechmann L, Clark M, Waldmann H, Winter G (March 1988). "Reshaping human antibodies for therapy". Nature 332 (6162): 323–327. Bibcode:1988Natur.332..323R. doi:10.1038/332323a0. PMID 3127726.
5 Chadd HE, Chamow SM (April 2001). "Therapeutic antibody expression technology". Curr. Opin. Biotechnol. 12 (2): 188–94.doi:10.1016/S0958-1669(00)00198-1. PMID 11287236

Goal-oriented, time line driven scientist, proficiently trained in different academic institutions in Germany, France and the USA. Experienced in the life sciences e-commerce environment with a focus on product development and customer relation management.
Aller à la page de l’auteur



